Des doigts d’hydrogel dont la lumière contrôle la déformation
Des actionneurs obtenus à partir d’hydrogel (chaînes de polymères gonflées d’eau) sont prometteurs de nombreuses applications en biologie, en médecine, en micro-fluidique et même en robotique. En effet, ces composés peuvent fournir des mouvements rapides, réversibles et à vitesse réglable, fort recherchés dans ces domaines. Eddie Wang, Malav S. Desai, et Seung-Wuk Lee, de l’University of California et du Lawrence Berkeley National Laboratory, à Berkeley, USA, ont mis au point de tels composés en interfaçant des chaînes de polypeptides du type de l’élastine avec des feuilles de graphène. Les mouvements de ces nano-composés sont contrôlés par excitation lumineuse dans le proche infrarouge.
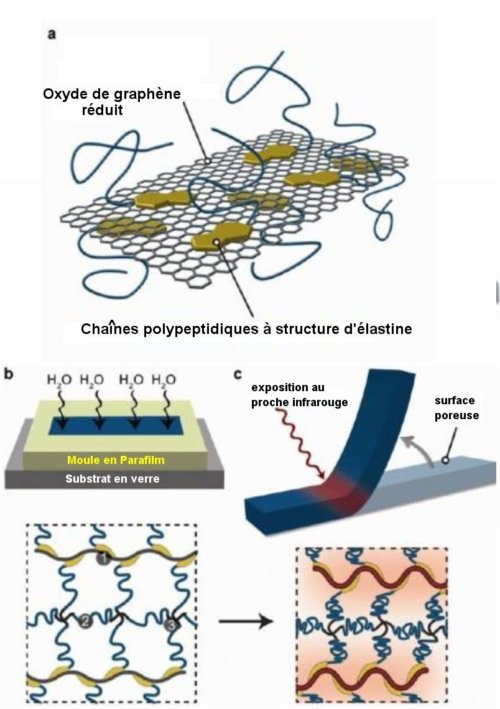
Fig.1.Méthode d’obtention d’un actionneur en hydrogel.
a) Accrochage de chaînes polypeptidiques du type élastine sur
une couche d’oxyde de graphène réduit. b) L’exposition à la
vapeur d’eau durant l’établissement des liaisons croisées
induit une anisotropie de porosité du gel. c) Schéma de
la courbure de cet hydrogel anisotropique sous l’effet d’une
illumination dans le proche infra-rouge. On a figuré
au-dessous le dégonflement local correspondant du réseau du gel. Crédit Nano letters, ©ACS
La combinaison des propriétés du graphène et de l’hydrogel donne réactivité et réversibilité aux actionneurs
L’utilisation de la lumière pour contrôler le mouvement de ces actionneurs permet d’éviter l’introduction de fils ou d’électrodes invasives. Ici, c’est l’anisotropie de porosité qui est exploitée : sous l’effet de la lumière le gel perd de son eau en surface ce qui entraîne sa contraction. Cet effet est rapide et parfaitement réversible. Ces qualités sont obtenues grâce à la combinaison des nano-feuilles de graphène et des chaînes de polypeptides synthétisés de type élastine.
Le graphène (cfle blog des sciences du 16 mars 2011) est un cristal hexagonal de carbone plan dont l’épaisseur est celle d’un atome. L’empilement de telles feuilles d’une extrême finesse constitue le graphite.
Le graphène est obtenu ici par réduction de graphite exfolié puis oxydé. Comme il absorbe bien le proche infrarouge, il va générer de la chaleur avec beaucoup d’efficacité. C’est celle-ci qui va entraîner la courbure de l’hydrogel.
Les chaînes de polypeptides genre élastine sont obtenues par synthèse en combinant des motifs d’acides aminés semblables à ceux existant dans la protéine animale tropo-élastine, précurseur de l’élastine des mammifères.
La surface exposée à la vapeur d’eau durant la polymérisation des chaînes de polypeptides est d’une porosité accrue. Cette région poreuse absorbe 4 fois plus d’eau que la région restante de faible porosité. Mais la diffusion de l’eau en entrée ou en sortie y est aussi quatre fois plus rapide que dans la région moins poreuse. C’est ce qui entraîne une courbure rapide du gel lors du gonflement ou dégonflement de cette couche poreuse.Ces actionneurs à base d’hydrogel peuvent être incorporés dans des systèmes nanoscopiques.
Des démonstrations impressionnantes
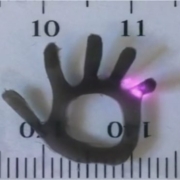
Dans ce but, les chercheurs ont réalisé une main miniature en hydrogel sur lequel ils ont fait agir un spot laser infrarouge.
La vidéo suivante montre les mouvements obtenus :
[jwplayer mediaid= »14378″]
La graduation vaut 1mm. Crédit Nano letters, ©ACS
Ils ont aussi placé face poreuse en dessous un hydrogel moulé avec une légère courbure. Un faisceau laser est utilisé pour augmenter la courbure d’une région du gel. A l’arrêt du laser, l’hydrogel recouvre sa courbure initiale et se propulse vers l’avant. On obtient ainsi un mouvement de reptation linéaire que l’on peut observer sur la vidéo ci-dessous :
[jwplayer mediaid= »14382″]
La graduation vaut 1mm. Crédit Nano letters, ©ACS
En incorporant des nanofeuilles de graphène dans des hydrogels à porosité anisotropique obtenus à partir de polypeptides synthétisés du genre élastine , on obtient des éléments capables de mouvements de torsion rapides, réversibles et d’intensité réglable en des positions spécifiées. Ceci montre tout l’intérêt de l’effet de synergie obtenu en combinant des polymères à base de protéines avec des nanomatériaux synthétiques tels que le graphène.
On peut imaginer d’appliquer cette stratégie à d’autres nanoparticules. On pourrait avec des dispositifs de ce genre contrôler par la lumière des cultures cellulaires, délivrer in situ des médicaments ou encore commander des systèmes microfluidiques et des minuscules robots.
Pour en savoir plus : Light-Controlled Graphene-Elastin Composite Hydrogel Actuators, Eddie Wang, Malav S. Desai, and Seung-Wuk Lee*, Nano Lett. May 2013 doi/10.1021/ nl401088b