Une avancée majeure vers un vaccin contre le SIDA
On sait depuis près de 20 ans que, sur mille personnes porteuses du virus VIH, virus de l’immunodéficience humaine, HIV en anglais, 3 en moyenne sont des porteurs sains du virus car ce dernier ne se multiplie pas au sein des lymphocytes CD4+T, cellules cibles du virus. Ces patients appelés en anglais » elite controllers « , abrégé en EC) conservent donc une immunité normale sans thérapie antivirale et ne sont pas contaminants.
Le mystère de cette absence de réplication du virus chez ce petit groupe de patients infectés vient d’être levé par deux chercheurs français, Jean Marie Andrieu et Wei Lu, associés a une équipe de cliniciens chinois .
Ils ont démontré que ces patients induisaient non pas des anticorps neutralisants mais une population de cellules CD8+T (dites régulatrices) qui inhibent l’activité des cellules CD4+T infectées par le VIH et de ce fait suppriment la réplication du virus au sein de ces cellules.
L’equipe française avait préalablement montré chez des singes macaques chinois qu’un vaccin oral fait à partir de virus inactivé de l’immunodéficience du singe (VIS) et de Lactobacillus plantarum (ou rhamnosus) protégeait de l’infection par VIS, non par des anticorps, mais grâce a l’induction du même type de lymphocytes CD8 régulateurs (voir le blog du 22 Jan 2013: Un vaccin révolutionnaire sans anticorps qui protège les macaques du virus VIS analogue du SIDA).
Parmi 3000 patients infectés du VIH suivis à Xishuanghanna au Yunnan, en Chine, on a trouvé dix EC (contrôleurs du VIH, en français) volontaires pour l’étude. Ces dix sujets étaient porteurs des protéines KIRD3L1 sur le chromosome 9 et avaient un profil génétique caractérisé par des antigènes des leucocytes humains (en abrégé HLA, de l’anglais human leukocyte antigen) HLA-B-Bw4-80 sur le chromosome 6.
Un gène est constitué d’une suite de fragments unitaires de l’ADN. Dans une cellule diploïde humaine, il y a 22 paires de chromosomes plus une 23ième déterminant le sexe. Chaque gène existe en 2 exemplaires, un allèle hérité du père, l’autre de la mère. Quand deux tels allèles présents sur un chromosome n donné, on dit que les gènes sont homozygotes. Dans le cas contraire, ils sont dits hétérozygotes.
On appelle allèle toute variante existante d’un gène donné.
Le protocole a consisté a tester in vitro l’activité antivirale de cellules CD8+T extraites ex vivo des dix EC sur des cellules CD4+T de la même origine infectées par le VIH ainsi que, pour comparaison, sur des cellules CD4+T infectées par le VIH provenant de patients atteints du VIH ou de porteurs sains.
L’action des CD8+ T sur les CD4+ T infectés par le VIH
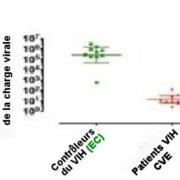
Dans le cas de 9 « contrôleurs du VIH »(ou EC) possédant le HLA-B-Bw4-80 et le gène KIR3DL1, on fait agir in vitro les cellules CD8+T fraichement extraites de leur sang sur leurs CD4+T surinfectées par le VIH. La concentration d’ARN viral est alors réduite d’un facteur >105 (Fig.1, points verts).
On observe une plus faible réduction (1000) de la charge virale sur un dixième EC, qui porte le KIR3DL1, mais chez qui le HLA-B-Bw4 est remplacé par un HLA-B-Bw6.
Au contraire, sur les CD4+ T venant de 10 patients atteints du VIH avec une charge virale élevée (CVE), la réduction de la charge virale par les CD8+T est très faible,≤100 (Fig.1, points marrons).
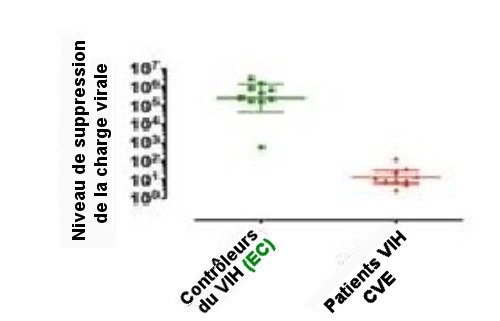
Fig. 1 Suppression in vitro de la charge virale par des cellules CD8+ T , en vert, chez 10 « contrôleurs du VIH »(EC) et, en marron, chez 10 patients ayant une charge virale élevée de VIH (CVE). Sur le contrôleur du VIH n°6, on observe une plus faible réduction de la charge virale. Cet EC n°6, porteur du KIR3DL1, ne l’était pas du HLA-B-Bw4, mais du HLA-B-Bw6. Reproduit de Frontiers in Immunology, 10 April 2016
Les caractéristiques génétiques propres aux EC
Parmi les dix « contrôleurs du VIH » (EC), les cellules mononucléaires extraites de leur sang portaient, pour 4 d’entre eux, le motif sérologique Bw4, pour 5 autres, le motif Bw4 et le motif Bw6, enfin pour l’un d’eux le n°6, le motif Bw6 seulement. Pour les 9 EC qui présentaient le motif Bw4, on trouvait en outre qu’ils portaient un résidu d’isoleucine (HLA-B:Bw4-80Ile)
Pour ce qui est des 10 porteurs de VIH à charge virale élevée (CVE), 7 d’entre eux portaient le motif Bw6; les trois autres portaient le Bw6 et le Bw4.
On remarque que 3 allèles des HLA (HLA-B 45Thr, 80Ile et HLA-A97Met sont beaucoup plus fréquents dans les EC que dans les patients CVE. C’est ce que l’on peut voir sur la figure 2 A ci-dessous. Pour les allèles KIR, la figure 2 B montre qu’ils sont plus fréquents chez les EC que chez les patients CVE.
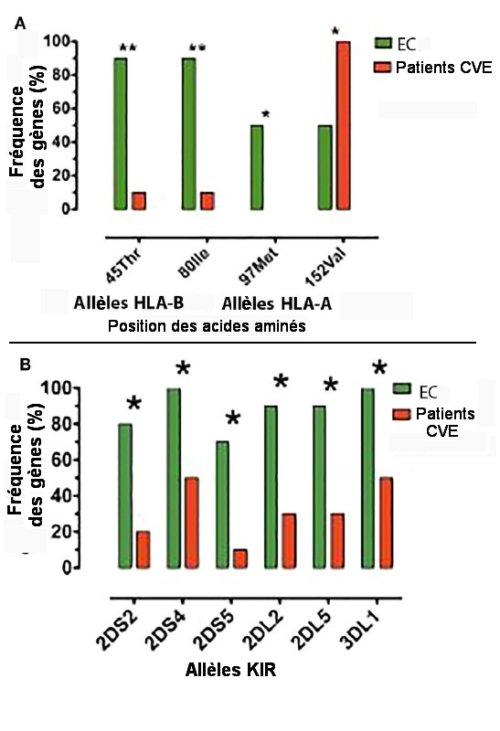
Fig.2. Différences de fréquences des allèles HLA et KIR entre 10 « contrôleurs du VIH » (EC) et 10 patients atteints du VIH avec une charge virale élevée. A) Des allèles HLA-A et HLA-B sont plus fréquents chez les EC que chez les patients CVE.
B) 5 allèles KIR sont plus fréquents chez les EC que chez les patients CVE. Reproduit de Frontiers in Immunology, 10 April 2016.
Les conclusions d’expériences sophistiquées
Les chercheurs ont effectué des tests plus détaillés de l’action des CD8+T sur les CD4+T menés sur les cellules mononucléaires extraites du sang de « contrôleurs du VIH », de patients atteints du VIH à CVE et de donneurs sains ayant divers profils génétiques. Ils ont ainsi montré qu’on obtenait une suppression de l’activation du virus VIH dans des cellules CD4+T portant le gène HLA-B:Bw4-80Ile par des cellules CD8+T portant le KIR3DL1.
Plus précisément, c’est la liaison des molécules de KIR3DL1 situées à la surface des CD8+T avec le peptide HLA-B:Bw4-80Ile porté par la surface des CD4+T infectées par le VIH qui supprime l’activation et la réplication du VIH dans les cellules CD4+T.
Ces résultats montrent que, chez la plupart des « contrôleurs du VIH », la suppression de la réplication du virus HIV dépend spécifiquement de caractères génétiques régissant l’interaction des cellules lymphocytes CD8+T avec leurs cibles, les lymphocytes CD4+T infectés par le virus. En rapprochant ceci du fait que ce sont justement des cellules CD8+T régulatrices qui sont induites par la vaccination des macaques chinois, on voit que cette découverte ouvre de grands espoirs pour la réalisation d’un vaccin efficace contre le HIV chez l’Homme.
.
Pour en savoir plus :
Suppression of HIV replication by cD8+ regulatory T-cells in elite controllers
Wei Lu, Song Chen, Chunhui Lai, Mingyue Lai , Hua Fang, Hong Da, Jun Kang, Jianhua Fan, Weizhong Guo, Linchun Fu and Jean-Marie Andrieu;
Frontiers in Immunology, 18 Avril 2016. doi:10.3389/fimmu.2016.00134