Une méthode de capture du CO2 facile à mettre en œuvre
Le changement climatique est dû principalement aux émissions de dioxyde de carbone CO2. Celles des centrales électriques utilisant des combustibles fossiles sont très importantes. Il est donc nécessaire d’épurer le CO2 des résidus gazeux de combustion qu’il contient . De nombreuses technologies ont été envisagées dans ce but, mais elles exigent un chauffage à vapeur qui oblige de rajouter aux installations des tuyauteries compliquées . De tels systèmes ne sont en outre pas économiquement faisables. Des chercheurs du MIT (Massachusetts Institute of Technology), Cambridge, U.S.A., ont mis au point un procédé électrochimique qui n’exige pas d’injection de vapeur, qui fonctionne à basse température, et surtout peut se rajouter extrêmement facilement à une installation préexistante.
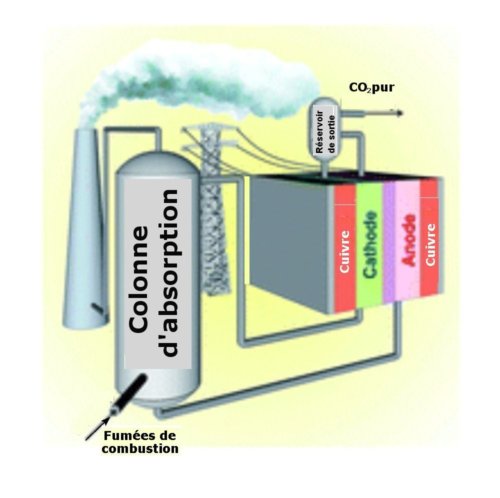
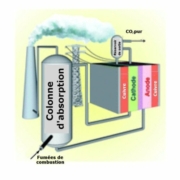
Fig.1. Vue d’artiste de la méthode électrochimique de séparation
du CO2 des gaz issus de la combustion d’une usine.
Crédit Energy & Environmental Science. © RSC.
Extraction du CO2 des fumées par une solution aqueuse d’amine
En sortie des brûleurs de l’installation, on dispose une colonne d’absorption contenant une solution aqueuse d’amine qui forme à température ordinaire avec le dioxyde de carbone un composé stable.
Les fumées ainsi débarrassées du CO2 sont évacuées dans l’atmosphère. Il reste à séparer le CO2 de la solution d’amine pour récupérer celle-ci et la réinjecter dans la colonne d’absorption. A la différence des techniques antérieures faisant appel à un chauffage par vapeur (Fig.2.) dispendieux en énergie et exigeant des modifications complexes de tuyauteries, les chercheurs du MIT ont proposé un procédé (Fig. 1. & 3) de régénération d’amine par voie électrochimique (en anglais Electrochemically Mediated Amine Regeneration, EMAR). Celui-ci combine l’avantage de l’absorption par solution aqueuse d’amine avec la facilité d’implantation d’un système électrique de récupération de l’amine. En outre, la consommation d’énergie est beaucoup plus faible avec un procédé électrochimique.
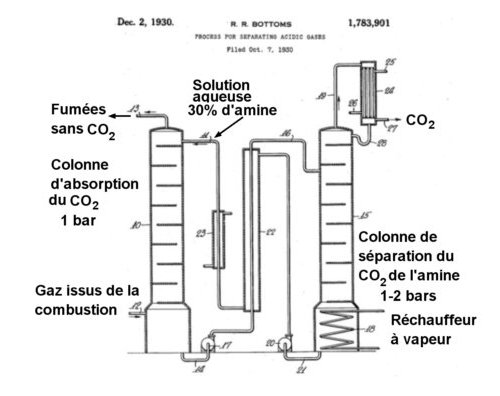
Fig.2. Schéma du procédé d’épuration des fumées d’usine du CO2 proposé par Bottoms en 1930. Ce système est trop gourmand en énergie et entraîne des modifications de circuit complexes et onéreuses. Crédit US Patent
Dans le système EMAR, l’étage d’absorption du CO2 par une solution d’amines est analogue à celui du procédé thermique. Après celui-ci, une pompe met sous pression la cellule électrochimique, ce qui permettra d’évacuer le gaz CO2 sous une pression de 10 bars. L’anode et la cathode sont toutes les deux en cuivre divisé, ce métal se combinant transitoirement aux amines dans la réaction électrochimique de séparation du CO2. Les cellules électrochimiques peuvent être empilées en parallèle pour diminuer les pertes par effet Joule.
Une membrane d’échange d’anions sépare la cathode de l’anode. Le CO2 va du côté de l’anode, les amines du côté de la cathode.
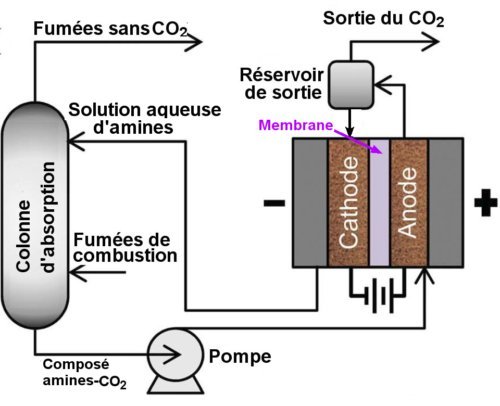
Fig.3. Schéma de la méthode électrochimique EMAR de récupération du dioxyde
de carbone proposée par les chercheurs du MIT.
Crédit Energy & Environmental Science. © RSC.
Les avantages du nouveau système
Un appareillage modèle a été construit et testé au laboratoire. Les résultats en ont été très encourageants. Le système électrochimique fonctionne à température ambiante et consomme bien moins d’énergie que le système thermique. Ce dernier caractère tient au fait que le système électrochimique agit seulement sur les molécules concernées à la différence du procédé thermique qui doit agir en outre sur le milieu les contenant.
Cette technique devrait être capable de retirer 90% du CO2 des rejets d’une centrale. Alors que le système thermique nécessite environ 40% de l’énergie produite par l’installation, le nouveau système ne devrait consommer que 25% de cette énergie. En outre, tandis que le système thermique à vapeur doit fonctionner de façon continue, le nouveau système peut être arrêté durant les périodes de pointe.
Comme le système électrochimique n’utilise pas de vapeur, on peut l’installer dans des usines qui n’en produisent pas, comme les cimenteries qui sont parmi les plus grandes productrices de rejets de CO2. Ceci pourrait aussi s’appliquer aux aciéries et aux usines d’aluminium. On pourrait même l’utiliser dans les sous-marins ou les vaisseaux spatiaux où le dioxyde de carbone doit être constamment éliminé pour permettre la vie à bord.
Le CO2 ainsi isolé doit être ensuite, soit séquestré dans des réservoirs géologiques, soit utilisé dans l’industrie à partir de bouteilles hautes pression.
Pour en savoir plus :
Post-combustion carbon dioxide capture using electrochemically mediated amine regeneration,
Michael C. Stern, Fritz Simeon, Howard Herzogb and T. Alan Hatton,
Energy & Environmental Science, Juin 2013, DOI: 10.1039/c3ee41165f